仅使用 1300 nm 激发的多探针三光子成像
一体化 1300 nm 光源使研究机构能够真正更深入地研究哺乳动物神经科学,同时激发短波和长波荧光探针。
2022 年 8 月 29 日,作者: Coherent
荧光蛋白和探针的三光子 (3P) 激发目前引起了人们的极大兴趣,尤其是在神经科学应用领域。 正如 Chris Xu 和其他研究人员所证实的那样,一个重要原因是用于三光子激发的 1300 nm 和 1700 nm 波长窗口中的长穿透深度。
三光子激发还可以提供比双光子激发更高的信噪比,并且几乎没有离焦荧光。这就可以穿透> 1 mm 厚的大脑皮层,在活体小鼠大脑中进行更深入的成像。
同样重要的是,1300 nm 波长符合绿色荧光蛋白和探针(如葡聚糖)的三光子激发能量要求,而 1700 nm 可用于激发更长波靶向,如 tdTomato。
一些研究人员希望同时激发多个探针以对哺乳动物大脑进行更复杂的探查。 这种信息丰富的数据可以加速研究人员了解神经连接和活动与重要功能之间关系的进程。
使用两种激发波长可以同时对短波和长波探针进行成像。 但是,这有一些限制。 首先,产生两种波长的光束并在显微镜中合并它们会很复杂(且会产生费用)。 然后是功率负荷问题;使用两个激光源来激发活体组织意味着要在样品上使用两倍的激光功率。 此外,直到最近,还没有针对 1300 nm 或 1700 nm 的简单(即“一体化”)光源,因此研究人员通常会使用 1040 nm 左右的激光来泵浦可调谐 OPA产生1300nm或1700nm。
但是两种发展的结合使得短波和长波探头的同时三光子激发变得更加简单,从而可以被更广泛的用户所接受。
1300 nm 激发长波探针
最近的几项三光子成像研究表明,1300 nm 可用于激发绿色和红色荧光探针。 然后使用过滤器在两个相机中分别检测来自两个探针的光。 例如,Timo van Kerkoerle 和他的博士生 Marie Guillemant 使用Monaco 和 Opera-F产生 1300 nm激光,演示了通过三光子激发在小鼠前额叶皮层中同时激发葡聚糖和 tdTomato 标记的中间神经元(图 1)。 此处的 z 堆栈图像显示,红移探针激发信号甚至在深度约为 1 mm 时也很显著。
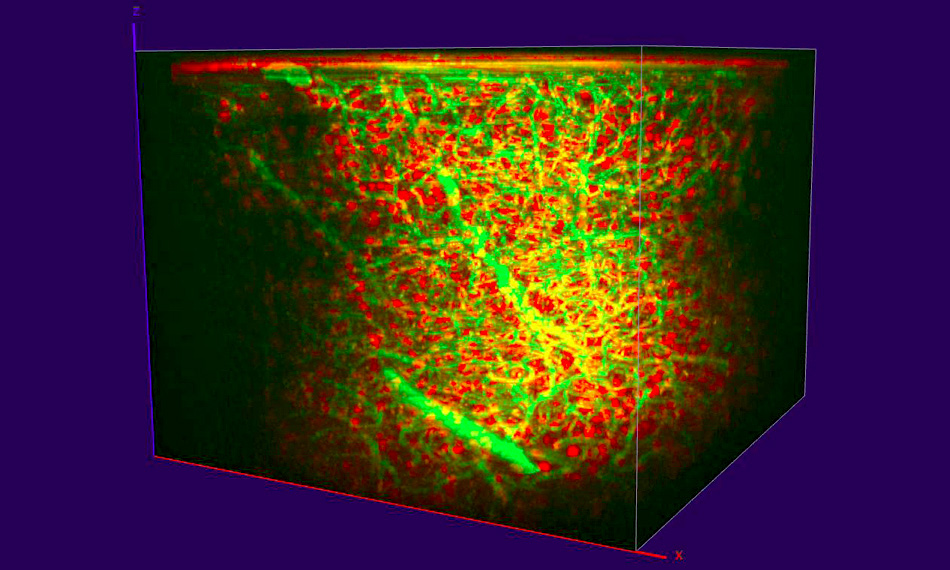
数据由 Timo van Kerkoerle 博士和 Marie Guillemant 提供,Neurospin,CEA Saclay。
图 1. 小鼠前额叶皮层中葡聚糖(绿色)和 tdTomato(红色)标记的中间神经元的三光子成像,深度约为 1 mm。
Chris Xu 在 2021 年发表了一篇关于多色荧光团单波长三光子激发的文章。*
这项工作表明,许多常用的红色荧光分子通常使用 1700 nm 激发成像到最低能量激发态,也可以在 1300 nm 激发到更高能量电子态。 这种新颖的激发机制允许仅使用 1300 nm 激光在小鼠大脑中进行双重绿色和红色三光子荧光成像。
我们相信 Timo van Kerkoerle 和 Chris Xu 的这些发现显然会对成像和功能性荧光探针的三光子激发的未来发展方向产生影响。
一体化 1300 nm 脉冲光源
另一个有用的进步是最近开发的一体式激光器,可为三光子激发提供最新型的 1300 nm 飞秒光源。 新推出的 Coherent Monaco 1300 就属于这种类型,它是一个简单易用的自动化光源,脉冲宽度小于 50 fs。
这种短脉冲宽度非常适合三光子成像,因为它可以产生高峰值功率,而 三光子图像亮度与激光峰值功率的三次方成正比。 这种新型激光器还提供高达 2.5 W 的输出,可选择 1、2 或 4 MHz 重复频率,支持快速图像采集。 此外,激光器具有高质量 (M2 <1.3) ,在三维上都能最大限度提高显微镜的吞吐量、成像效率和图像分辨率。
一体化结构还包括两个常用功能选件,可以简化三光子成像并提高图像亮度。 这两个选件分别是提供动态功率衰减/门控的全功率控制 (TPC) 功能,以及提供色散预补偿以在样品处获得最佳脉冲宽度的紧凑型脉冲压缩器 (CPC)。
三光子成像的美好未来
使用单个激光源激发多个探针有望推动神经科学领域的发展,该技术基于跨皮层深层映射多种细胞类型,实现对大脑容量的快速、信息丰富的成像。 三光子激发技术和相关机制的发展无疑有助于为正在决定选择可调谐还是单波长三光子激发光源的研究人员提供指引,并突出(如 Coherent Monaco 1300)解决方案的价值。
在我们的博客中了解更多关于 Coherent Monaco 1300 的信息。
* 来源: 小鼠脑深部单波长激发的多色三光子荧光成像,Science Advances。

